RESUMEN
Antecedentes: El cáncer gástrico en la mujer embarazada tiene una incidencia de entre 0.026% y 0.1%. El diagnóstico suele establecerse en etapas avanzadas, lo que contribuye a un pronóstico desfavorable.
Caso clínico: Paciente de 32 años, con antecedentes de: legrado por aborto retenido (2021), salpingooforectomía izquierda por quiste torcido de ovario izquierdo (2022), conización por NIC III (2023), colelitiasis y antecedente materno de cáncer de mama; dos embarazos y un aborto, en curso de las 23.1 semanas de la gestación actual. Acudió a urgencias debido a un cuadro de dos días de evolución, de episodios eméticos de hemorragia digestiva alta, asociados con dispepsia, pirosis y pérdida de 4 kg en el último mes. La endoscopia digestiva alta evidenció la existencia de una lesión tumoral antral en el conducto pilórico hasta la primera porción del duodeno, de aspecto mucinoso, que provocaba estenosis pilórica secundaria. Para disminuir la estenosis pilórica y poder lograr la nutrición enteral y posterior quimioterapia paliativa se decidió la colocación de un stent duodenal por vía endoscópica.
Conclusión: La trascendencia del reporte se apoya en comunicar la experiencia que, por lo menos, en algo contribuya a la ausencia de guías clínicas específicas de tratamiento, con necesidad de atención multidisciplinaria, toma de decisiones individualizadas, prioridad de la supervivencia de la madre y valoración de la salud del feto y la viabilidad del embarazo.
Palabras clave: Neoplasias gástrica, gravidez, quimioterapia adyuvante
ABSTRACT
Background: Gastric cancer during pregnancy is rare, with an incidence ranging from 0.026% to 0.1%. Typically, diagnosis occurs at an advanced stage, resulting in a poor prognosis.
Clinical case: A 32-year-old woman presented with a medical history including curettage for retained abortion (2021), left salpingo-oophorectomy for ovarian torsion (2022), conization for CIN III (2023), cholelithiasis, and a maternal history of breast cancer. She has experienced two pregnancies and one abortion, and is currently at 23.1 weeks gestation. The patient sought emergency care due to two days of vomiting episodes accompanied by upper gastrointestinal bleeding, along with dyspepsia, heartburn, and a recent weight loss of 4 kg over the past month. Upper gastrointestinal endoscopy revealed a mucinous antral tumor lesion located in the pyloric canal, extending into the first portion of the duodenum and causing secondary pyloric stenosis. To alleviate the obstruction and facilitate enteral nutrition followed by palliative chemotherapy, an endoscopic duodenal stent was placed.
Conclusion: This report highlights the importance of documenting such cases, given the lack of specific clinical guidelines for treatment. It underscores the necessity of multidisciplinary management, individualized therapeutic decisions, prioritizing maternal survival, and ongoing evaluation of fetal health and pregnancy viability.
Keywords: Gastric neoplasms, Pregnancy, Adjuvant chemotherapy
ANTECEDENTES
El cáncer gástrico ocupa el sexto lugar mundial de todas las neoplasias, con diferencias poblacionales, geográficas y socioeconómicas. La edad promedio a la aparición es de 50 años, con predominio del género masculino. Los factores de riesgo son hereditarios, exposición al tabaco y antecedentes de reflujo gastroesofágico, úlcera gástrica, infección por Helicobacter pylori o enfermedad inmunosupresora.1,2 Es poco común en mujeres en edad fértil; en la gestación o posparto complica entre el 0.026 y el 0.1% de los embarazos, sin que existan datos exactos de su incidencia en este grupo poblacional 1,3. Se ha encontrado un vínculo con la alimentación rica en dietas con sal, conservantes y carnes rojas. Su relación con H. pylori aumenta, incluso, 10 veces el riesgo de padecer cáncer gástrico; esta bacteria es el precursor más relevante del proceso de carcinogénesis.4 Desde el punto de vista histológico, el cáncer gástrico tiene diferentes formas de manifestación: intestinal (54%) asociada con factores ambientales y geográficos y difuso (32%) relacionado con causas genéticas y la indeterminada (10 a 12%).5
Según Isobe y colaboradores,6 el aumento de estrógenos y el estado inmunosupresor característicos del embarazo participan en su etiopatogenia. Su reconocimiento temprano es complejo porque los síntomas iniciales de la gestación: náuseas, vómitos y dispepsia se superponen,7 lo mismo que los cambios fisiológicos del embarazo, como el estado de hemodilución, con disminución de las concentraciones de hemoglobina y albúmina. A lo anterior se agrega la predisposición a un estado protrombótico por cambios en los factores de la coagulación.8
Si los síntomas gástricos persisten con pérdida de peso, melenas, hematemesis y anemia, se sugiere descartar una neoplasia maligna, con estudio endoscópico (esofagogastroduodenoscopia o colonoscopia) para establecer un diagnóstico oportuno.9 A su vez, deben practicarse estudios imagenológicos. La ecografía abdominal es una opción rápida y segura porque no expone al feto a la radiación ionizante.10 También puede recurrirse a pruebas más complejas: tomografía axial computada y la resonancia magnética nuclear, que estadifican la enfermedad y descartan complicaciones asociadas. Para evitar el riesgo de malformaciones se recomienda su práctica después del periodo de organogénesis. Está demostrado que una exposición menor a 50 mGy después del primer trimestre no tiene efectos relevantes en el feto.11 De igual manera, se tiene conocimiento de que el gadolinio, como medio de contraste, no se vincula con efectos teratogénicos.12
Posterior a la identificación debe procederse a la estadificación, conforme a lo señalado en la octava edición de la clasificación TNM de la American Joint Committee on Cancer (AJCC) y de la Union for International Cancer Control (2017), que se basa en invasión tumoral (T), afectación ganglionar (N) y metástasis (M). El cáncer gástrico suele clasificarse en dos grupos: temprano y avanzado. El cáncer gástrico temprano se limita a la mucosa o submucosa (T1), con una supervivencia a 5 años del 90%. El cáncer gástrico avanzado es una neoplasia maligna epitelial con origen en las glándulas de la mucosa gástrica, que afecta capas más profundas (T2-T4), con una supervivencia a 5 años del 7 al 27%.13
Las clasificaciones histológicas más utilizadas son la de Lauren y la Organización Mundial de la Salud (OMS). La primera divide al adenocarcinoma gástrico en tipo intestinal (54%), difuso (32%) e indeterminado (14%). El tipo difuso es más común en jóvenes y discretamente más frecuente en mujeres; afecta al cuerpo gástrico, con peor pronóstico. La clasificación de la OMS separa el adenocarcinoma gástrico en tubular, papilar y mucinoso.14
La atención médica de estas pacientes debe ser multidisciplinaria e integral, por sus implicaciones éticas, legales y psicológicas en la madre y su entorno familiar. Se considera un reto porque la vida de la madre prevalece cuando no es posible salvaguardar ambas; claro está que la decisión de la madre es decisiva en el desenlace de la gestación.1 La atención médica dependerá de la etapa del diagnóstico, cuando es temprana la indicación primaria es la cirugía mediante gastrectomía, con intención curativa. En estadios localmente avanzados la opción es la quimioterapia neoadyuvante seguida de la cirugía y en estadios avanzados (metastásico o irresecable) la quimioterapia paliativa.15
La decisión del procedimiento quirúrgico dependerá de la estadificación y las semanas de gestación transcurridas.1 Hasta las 22 semanas, en estadios tempranos, se recomienda la resección endoscópica; y si la afectación de la madre lo exige se optará por una cirugía mayor, con la posible pérdida gestacional, con bajo riesgo de muerte de la madre (menos de 1 por cada 10,000).16 Entre las 22 y 28 semanas el panorama para el feto mejora con una resección quirúrgica luego de la finalización del embarazo mediante cesárea. Después de las 28 semanas el nacimiento puede ocurrir por parto o cesárea y, aproximadamente, 15 días después se hará la resección, para disminuir la morbilidad y mortalidad de la madre.17
En los casos de neoplasias avanzadas, complicadas por perforación o hemorragia, lo indicado es la resección paliativa, con el fin de preservar la vida de la madre, pero con aumento del riesgo de pérdida del feto. También se dispone de maniobras terapéuticas conservadoras, como la inyección de epinefrina, termocoagulación y electrocoagulación mediante imagenología, para disminuir la hemorragia de vías digestivas y los síntomas.
La quimioterapia es un agente citotóxico durante el embarazo, la FDA lo clasifica en las categorías C (no se puede descartar riesgo) y D (existe riesgo para el feto). El esquema más indicado es una combinación de platino y fluoropirimidina, como folfox (5-fluorouracilo, leucovorina, oxaliplatino). En referencia a la dosis, no existen recomendaciones diferentes a las de la población general; solo deben hacerse ajustes según el peso corporal y las semanas de gestación.18 Los riesgos de daño al feto disminuyen conforme avanza el embarazo. A partir del segundo trimestre se recomienda disminuir el riesgo de malformaciones, carcinogénesis y retraso en el desarrollo.19
Con estudios limitados en cáncer gástrico se indica la quimioterapia, que debe administrarse, de preferencia, hasta las 33 semanas con tiempo libre de 3 semanas entre el parto y la aplicación para evitar la aplasia medular en los recién nacidos. Desde luego, también puede recurrirse a la inmunoterapia.21
Los desenlaces de la madre y el feto se asocian con un diagnóstico en etapa avanzada y una histología pobremente diferenciada, con una supervivencia a los 3 años del 23.3%.22 A su vez, se ha evidenciado una relación entre preeclampsia y el diagnóstico oncológico, lo que obliga a finalizar la gestación antes de lo previsto.3 La propagación de células tumorales de la madre al feto es poco común, debido a que el sincitiotrofoblasto actúa como la primera barrera de protección; sin embargo, la invasión a las vellosidades placentarias aumenta el riesgo de metástasis al feto.
Por lo anterior, es decisivo examinar la placenta, y si se encuentra afectada, deberá estudiarse la metástasis durante el periodo neonatal y la infancia.23 La supervivencia del feto es más favorable, con un pronóstico del 77%. Los fetos menores de 28 semanas son los más sensibles al aborto, parto prematuro y muerte intrauterina. Mientras que los mayores de 30 semanas alcanzan una tasa de supervivencia cercana al 100%.24 La mayoría de los recién nacidos ingresan a la unidad de cuidados intensivos neonatales debido a la prematurez y bajo peso al nacer; a pesar de esto, no hay evidencia de desenlaces neonatales adversos si los esquemas de tratamiento se administraron después de la organogénesis.3
CASO CLÍNICO
Paciente de 32 años, procedente de Nariño, con antecedente de dos embarazos y un aborto, en curso de las 23.1 semanas de la gestación actual, con historial de colelitiasis, conización por NIC III (2023), salpingooforectomía izquierda por quiste torcido de ovario izquierdo (2022), legrado por aborto retenido (2021) y antecedente materno de cáncer de mama. Ingresó al hospital debido a un cuadro de dos días de evolución de episodios eméticos, asociado con dispepsia, pirosis y pérdida de 4 kg en el último mes.
En el reporte ecográfico abdominal del hospital local se evidenciaron las lesiones hepáticas y la tumoración intraperitoneal de 47 x 40 mm en el epigastrio y adenopatías adyacentes al tronco celiaco, con alta sospecha de proceso neoproliferativo. Los estudios paraclínicos reportaron: anemia moderada ferropénica (hemoglobina 7.6 mg/dL, volumen corpuscular medio: 93.3), hiponatremia, función hepática y renal adecuada y albúmina (2.7 g/dL).
La endoscopia de vías digestivas altas evidenció la existencia de una lesión tumoral antral en el conducto pilórico que abarcaba hasta la primera porción del duodeno, de aspecto mucinoso, con estenosis pilórica secundaria. En la resonancia magnética del abdomen se advirtieron las metástasis hepáticas, adenopatías retroperitoneales y peripancreáticas, la lesión tumoral de 4.9 x 5.1 cm en contacto con la curvatura menor del estómago y el cuerpo del páncreas. Se inició el tratamiento antiemético y el inhibidor de bomba de protones, además de transfusión de hemoderivados.
El reporte histopatológico fue de: cáncer gástrico, tipo adenocarcinoma mixto difuso (tubular e intestinal moderadamente diferenciado G3), con células en anillo de sello.
Se inició la intervención multidisciplinaria, por parte los perinatólogos, ginecoobstetras, intensivista, oncólogo clínico, cirujano oncólogo, neonatólogo, especialista en medicina del dolor y psicología. Se estableció el diagnóstico de cáncer gástrico en estadio avanzado (IV), con beneficio de quimioterapia paliativa. A la paciente se le explicaron los riesgos y beneficios e hizo hincapié en que la meta era preservar ambas vidas, siempre que fuera posible.
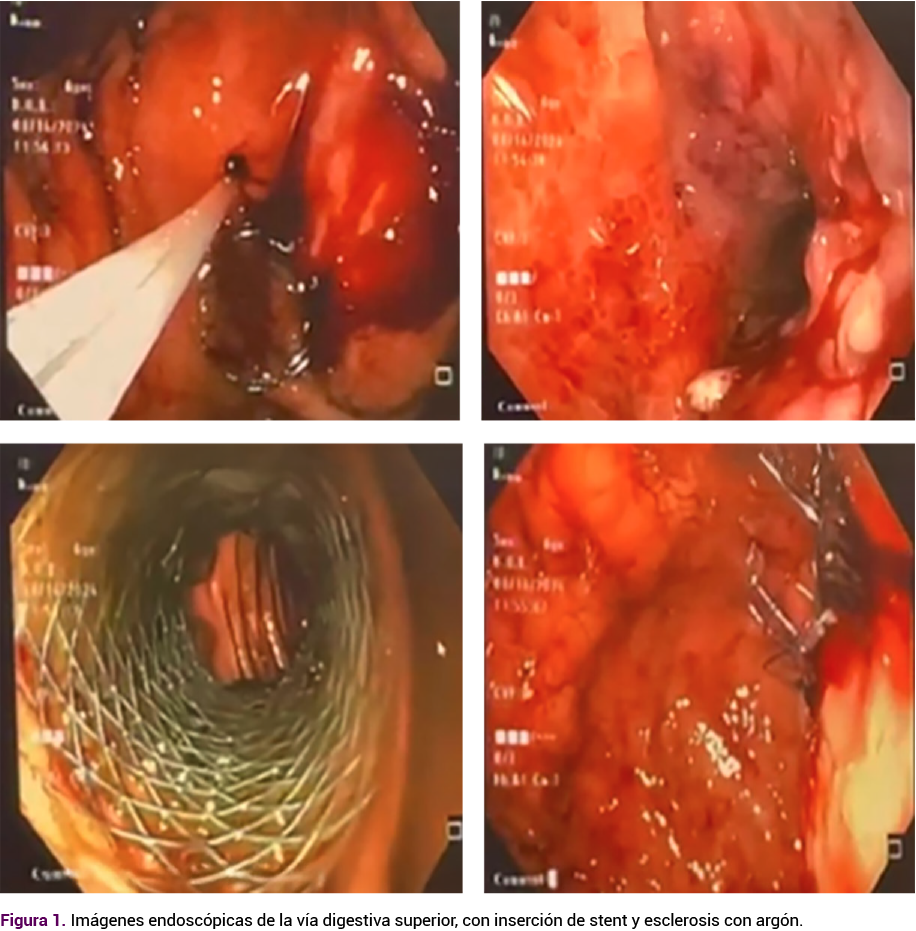
La evolución fue tórpida, por la persistencia de los episodios de hematemesis e intolerancia a la vía oral. Se le colocó un stent duodenal por vía endoscópica, para disminuir la estenosis pilórica y lograr la nutrición enteral (Figura 1); sin embargo, la paciente requirió la embolización de vasos cortos, dependientes de la arteria esplénica y múltiples transfusiones para lograr una hemoglobina óptima e iniciar el tratamiento neoadyuvante.
Con respecto al bienestar del feto, las ecografías obstétricas no evidenciaron alteraciones; sin embargo, 19 días posteriores al ingreso, la paciente tuvo cifras tensionales elevadas, sin rango de crisis (estadio I), y perfil endotelial con trombocitopenia leve (104,000 por microlitro) y hemólisis (LDH: 1.805, AST; 88 y ALT: 188). El Doppler fetal reportó anemia aguda; con estos parámetros se integró el diagnóstico de síndrome HELLP.
Se decidió la cesárea de urgencia, con hallazgos de focos de desprendimiento placentario, obtención de un recién nacido pretérmino de 25.5 semanas, sexo femenino, peso 750 g, APGAR 5-5 al minuto y a los 5 minutos, respectivamente. Se efectuaron las maniobras de reanimación e ingreso a la unidad de cuidados intensivos neonatales, donde la recién nacida permaneció hospitalizada durante 101 días, por prematurez extrema, anemia multifactorial, con requerimiento de varias transfusiones, foramen oval de 4.3 mm, retinopatía del prematuro estadio 2 zona II AO, sin avance y displasia broncopulmonar moderada; a quien se dio el alta del hospital.
Luego de la finalización del embarazo se registró la normalización de las pruebas hepáticas y plaquetas, sin nuevos eventos hipertensivos. Durante su permanencia en el hospital se inició el tratamiento neoadyuvante, con 10 sesiones de radioterapia y seis ciclos de quimioterapia e inmunoterapia con folfox-nivolumab en un periodo de seis meses.
Al mes, la paciente reingresó al hospital en malas condiciones generales, con hipotensión, taquicardia, dolor en el epigastrio y palidez mucocutánea asociada con hematemesis y melenas. Se consideró el choque hipovolémico secundario a hemorragia de vías digestivas altas; hemoglobina en 3.9 mg/dL y tiempos de coagulación prolongados. Recibió transfusión de 3 unidades de glóbulos rojos y plasma fresco congelado.
En la endoscopia, a través del stent, se observó una tumoración friable que se introducía al interior de este y no permitía el avance del instrumental al duodeno. Se procedió a la escleroterapia, con adrenalina al 1:20.000 UI y argón plasma para control del sangrado.
Durante su estancia tuvo varias complicaciones: coagulopatía, neumotórax derecho, trombosis de la vena subclavia, axilar y humeral, con deceso a los 11 días de su ingreso a pesar de las múltiples intervenciones; la familia decidió no practicar más medidas de soporte.
DISCUSIÓN
La frecuencia del cáncer gástrico en la población general varía según la ubicación geográfica y los factores de riesgo.25 Llega a afectar al 6.5% de personas menores de 40 años. Según GLOBOCAN (2022) Colombia se encuentra entre los países con mayor incidencia de cáncer gástrico en el mundo; ocupa el cuarto lugar, con una incidencia de 17.5 casos por cada 100,000 habitantes en la población femenina.26 Los estudios clínicos han demostrado que la aparición y evolución del cáncer gástrico en mujeres se relaciona con factores biológicos y hormonales,27 donde el predominio de los estrógenos contribuye a la aparición de células neoplásicas, sobre todo del tipo indiferenciado.28
El cáncer gástrico es una enfermedad de baja prevalencia en el embarazo, que se diagnostica en estadios avanzados debido a que los síntomas son similares a los de la gestación temprana,29 como se evidenció en el caso clínico aquí reportado y en una revisión de Zeng y Zhou30 en 2015 de 65 pacientes embarazadas con cáncer gástrico estadio IV.
Las características histológicas son similares a las observadas en mujeres no embarazadas; sin embargo, su pronóstico es desfavorable, según lo reportado por Lee y su grupo27 donde el 60% de los casos eran irresecables, lo que evidencia una tasa de supervivencia anual hasta del 46.7%. Este hallazgo durante el embarazo representa una situación preocupante para la madre y su familia, por ello se requiere de un acompañamiento multidisciplinario.31
La evaluación ecográfica puede detectar la enfermedad en etapas tempranas, y su aplicación está permitida en cualquier semana del embarazo; es necesario recurrir a estudios complementarios de tomografía axial computada y de resonancia magnética nuclear para estadificar la lesión.11,12 Por su parte, la endoscopia es decisiva para establecer el diagnóstico y tratamiento inicial del cáncer gástrico, como se confirma en el caso aquí reportado; es un procedimiento seguro en el embarazo, con un 95% de fetos sin complicaciones.28
El tratamiento con intención curativa solo se ofrece en etapas tempranas;16 como lo evidencian Sakamoto y otros32 con 136 casos donde solo el 43.5% se beneficiaron de una resección. La quimioterapia puede indicarse de forma neoadyuvante o paliativa según corresponda, lo que aumenta la supervivencia general de las pacientes.33 La administración en el primer trimestre aumenta el riesgo de aborto espontáneo, malformaciones y muerte del feto. Mientras que la administración en el segundo y tercer trimestre carece de riesgos significativos para el feto.34
El pronóstico de la madre y el feto va a estar relacionado, directamente, con el estadio del cáncer gástrico. Jeong Song y su grupo35 informaron que las bajas tasas de supervivencia general de estas pacientes se debieron a la etapa avanzada en el momento del diagnóstico asociado con el embarazo. Concluyeron que el diagnóstico temprano y el tratamiento quirúrgico son los únicos factores que pueden mejorar los desenlaces finales de este cáncer. Además, en el estudio de Maggen y colaboradores se evidenció la asociación entre cáncer gástrico y preeclampsia aguda o sus complicaciones, lo que conduce a la finalización de la gestación de manera prematura; así como ocurrió en la paciente del caso, por la concomitancia con síndrome HELLP.3
La supervivencia del feto aumenta conforme avanzan las semanas de gestación, con pocas repercusiones en la vida posnatal.24 La metástasis fetal es excepcional, aunque puede ocurrir debido a la inmadurez del sistema inmunológico.21 Altman y coautores sugieren que las metástasis placentarias deben considerarse estadio IV y tratarse como tal.23 En la paciente del caso, a pesar de la prematurez, la recién nacida logró superar su estancia en cuidados intensivos y en la actualidad se encuentra en buenas condiciones generales, sin evidencia de metástasis fetal.
CONCLUSIÓN
La relevancia del cáncer gástrico durante el embarazo radica en su excepcional frecuencia y en las dificultades para su diagnóstico, sobre todo cuando sus síntomas se confunden con los propios del embarazo, lo que retrasa su identificación. La mayoría de los casos diagnosticados en etapas avanzadas son irreversibles y requieren tratamiento con quimioterapia paliativa. Una intervención multidisciplinaria repercute de manera positiva en la supervivencia de la madre y en el pronóstico del feto y neonato.
AGRADECIMIENTOS
Al departamento de Ginecología y Obstetricia de la Universidad Libre -seccional Cali, Valle, Colombia y el Hospital Fundación San Pedro, Pasto, Nariño, Colombia.
DECLARACIONES
Conflicto de intereses
Los autores declaran no tener intereses contrapuestos.
Financiación
El proyecto se llevó a cabo con recursos propios.
Uso de inteligencia artificial
Los autores declaron no haber recurrido a la inteligencia artificial en ninguno de los apartados de este reporte de caso.
Referencias
- Constantin A, Constantin R, Achim F, Socea B, et al. Pregnancy and gastric cancer: a narrative review. Diagnostics (Basel) 2023; 13 (11): 1909. https://doi.org/10.3390/diagnostics13111909.
- Center MM, Jemal A, Smith RA, Ward E. Worldwide variations in colorectal cancer. CA Cancer J Clin 2009; 59 (6): 366-78. https://doi.org/10.3322/caac.20038.
- Maggen C, Lok CA, Cardonick E, van Gerwen M, et al. Gastric cancer during pregnancy: report of 13 cases and review of the literature with focus on chemotherapy during pregnancy. Acta Obstet Gynecol Scand 2020; 99 (1): 79-88. https://doi.org/10.1111/aogs.13731.
- Wen S, Moss SF. Helicobacter pylori virulence factors in gastric carcinogenesis. Cancer Lett 2009; 282 (1): 1-8. https://doi.org/10.1016/j.canlet.2008.11.016.
- Hu B, El Hajj N, Sittler S, Lammert N, et al. Gastric cancer: classification, histology and molecular pathology. J Gastrointest Oncol 2012; 3 (3): 251-61. https://doi.org/10.3978/j.issn.2078-6891.2012.021.
- Isobe T, Hashimoto K, Kizaki J, Miyagi M, et al. Clinicopathological characteristics and prognosis of gastric cancer in young patients. Oncol Rep 2013; 30 (1): 43-49. https://doi.org/10.3892/or.2013.2467
- Lee NM, Saha S. Nausea and vomiting of pregnancy. Gastroenterol Clin North Am 2013; 40 (2): 1-27. https://doi.org/10.1016/j.gtc.2011.03.009
- Tan EK, Tan EL. Alterations in physiology and anatomy during pregnancy. Best Pract Res Clin Obstet Gynaecol 2013; 27 (6): 791-802. https://doi.org/10.1016/j.bpobgyn.2013.08.001
- Ludvigsson JF, Lebwohl B, Ekbom A, Kiran RP, et al. Outcomes of pregnancies of women undergoing endoscopy while pregnant: a nationwide cohort study. Gastroenterology 2017; 152 (3): 554-63.e9. https://doi.org/10.1053/j.gastro.2016.10.016
- Copel J, El-Sayed Y, Heine RP, Wharton KR. Guidelines for diagnostic imaging during pregnancy and lactation. Am Coll Obstet Gynecol 2016; 656: 1-6. https://doi.org/10.1097/AOG.0000000000001316.
- Chen MM, Coakley FV, Kaimal A, Laros RK Jr. Guidelines for computed tomography and magnetic resonance imaging use during pregnancy and lactation. Obstet Gynecol 2008; 112 (2 Pt 1): 333-40. https://doi.org/10.1097/AOG.0b013e318180a505.
- Kanal E, Barkovich AJ, Bell C, Borgstede JP, et al. Expert Panel on MR Safety. ACR guidance document on MR safe practices: 2013. J Magn Reson Imaging 2013; 37 (3): 501-30. https://doi.org/10.1002/jmri.24011.
- López Sala P, Leturia Etxeberria M, Inchausti Iguíñiz E, Astiazaran Rodríguez A, et al. Gastric adenocarcinoma: a review of the TNM classification system and ways of spreading. Radiologia (Engl Ed) 2023; 65 (1): 66-80. https://doi.org/10.1016/j.rxeng.2022.10.011.
- Arias-Rodríguez FD, Ganchozo-Solís RV, Mosquera-López ED, Chávez-Pasquel DA, et al. Gastric cancer – update on diagnosis and treatment: a literature review. Rev Gastroenterol Latinoam 2024; 35 (3): 151-59. https://doi.org/10.46613/gastrolat2024003-06.
- ESMO Guidelines Committee. Gastric cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 2016; 27 (Suppl 5): v38-v49.
- Marbun VMG, Putranto AS. Diagnosis and treatment of gastric cancer in pregnancy: a case report based on evidence. Int J Surg Case Rep 2020; 75: 338-44. https://doi.org/10.1016/j.ijscr.2020.09.109.
- Okeagu CN, Anandi P, Gennuso S, Hyatali F, et al. Clinical management of the pregnant patient undergoing nonobstetric surgery: review of guidelines. Best Pract Res Clin Anaesthesiol 2020; 34 (2): 269-81. https://doi.org/10.1016/j.bpa.2020.04.004.
- Abdel-Rahman O, Ghosh S. Pregnancy and perinatal outcomes following exposure to antineoplastic agents during pregnancy in the FDA adverse event reporting system. Future Oncol. 2022; 18(23): 2635–2642. https://doi.org/10.2217/fon-2021-1255.
- Van Gerwen M, Maggen C, Cardonick E, et al. Association of chemotherapy timing during pregnancy with congenital malformations. JAMA Netw Open. 2021; 4(6): e2113180. https://doi.org/10.1001/jamanetworkopen.2021.13180.
- Triarico S, Rivetti S, Capozza MA, Romano A, et al. Transplacental passage and fetal effects of antineoplastic treatment during pregnancy. Cancers (Basel) 2022; 14 (13): 3103. https://doi.org/10.3390/cancers14133103
- Janjigian YY, Bendell J, Calvo E, Kim JW, et al. CheckMate-032 study: efficacy and safety of nivolumab and nivolumab plus ipilimumab in patients with metastatic esophagogastric cancer. J Clin Oncol 2018; 36 (28): 2836-844. https://doi.org/10.1200/JCO.2017.76.6212
- Tavares A, Gandra A, Viveiros F, Cidade C, et al. Analysis of clinicopathologic characteristics and prognosis of gastric cancer in young and older patients. Pathol Oncol Res 2013; 19 (1): 111-17. https://doi.org/10.1007/s12253-012-9530-z
- Altman JF, Lowe L, Redman B, Esper P, et al. Placental metastasis of maternal melanoma. J Am Acad Dermatol. 2003; 49(6): 1150-1154. https://doi.org/10.1016/S0190-9622(03)00124-5
- Cift T, Aydogan B, Akbaş M, Aydın B, et al. Case report: Gastric carcinoma diagnosed at the second trimester of pregnancy. Case Rep Obstet Gynecol 2011; 2011: 532854. https://doi.org/10.1155/2011/532854
- Jemal A, Bray F, Center MM, Ferlay J, et al. Global cancer statistics. CA Cancer J Clin 2011; 61 (2): 69-90.
- International Agency for Research on Cancer (IARC). GLOBOCAN 2022: Colombia fact sheet. Lyon (France): World Health Organization; 2024.
- Lee HJ, Lee IK, Kim JW, et al. Clinical characteristics of gastric cancer associated with pregnancy. Dig Surg 2009; 26 (1): 31-36. https://doi.org/10.1159/000193330.
- Kamani L, Achakzai MS, Ismail FW, Kayani F. Safety and outcomes of endoscopy during pregnancy. Cureus 2019; 11 (10): e6301. https://doi.org/10.7759/cureus.6301.
- Hussain N, Selvakumari N, Afadapa F, Amu O. Pregnancy and gastric cancer: diagnostic and treatment dilemma. BMJ Case Rep 2018; 2018: bcr2017222963. https://doi.org/10.1136/bcr-2017-222963.
- Zeng H, Zhou X, Xie H, Zhao Y, et al. Gastric cancer during pregnancy in China: case reports and a mini-review. J Surg 2015; 11: 165-68. https://doi.org/10.7438/1584-9341-11-4-9.
- Parangi S, Levine D, Henry A, Isakovich N, et al. Surgical gastrointestinal disorders during pregnancy. Am J Surg 2007; 193 (2): 223-32.
- Sakamoto K, Kanda T, Ohashi M, Kurabayashi T, et al. Management of patients with pregnancy-associated gastric cancer in Japan: a mini-review. Int J Clin Oncol 2009; 14 (5): 392-96. https://doi.org/10.1007/s10147-009-0903-6.
- Spiegel D, Palta M, Uronis H. Role of chemotherapy and radiation therapy in the management of gastric adenocarcinoma. Surg Clin North Am 2017; 97 (2): 421-35. https://doi.org/10.1016/j.suc.2016.11.013.
- Esposito S, Tenconi R, Preti V, Groppali E, et al. Chemotherapy against cancer during pregnancy: a systematic review on neonatal outcomes. Medicine (Baltimore). 2016; 95 (38): e4899. https://doi.org/10.1097/MD.0000000000004899.
- Song MJ, Park YS, Song HJ, Park SJ, et al. Prognosis of pregnancy-associated gastric cancer: a case-control study matched by age, sex, and stage. Gut Liver 2016; 10 (5): 731-38. https://doi.org/10.5009/gnl15323